日坛AI
生物医药研发的智能操作系统
破解数据孤岛与生物复杂性双重挑战,重塑从靶点发现到临床验证的研发范式
统一智能基座
原生集成14+国际主流生物信息学平台,无缝打通基因组、蛋白组、影像组等多尺度数据,构建可追溯、可计算的生物数据资产库
世界模型引擎
千亿参数生命科学大模型融合因果推理与联邦学习,模拟体内生物过程,提供可解释的预见性决策,超越传统相关性分析局限
端到端转化加速
支撑干湿实验闭环迭代,缩短从早期发现(Hit)到临床候选物(PCC)的转化路径,提供监管科学友好的完整证据链

洞察医疗盲区,挑战难愈之疾。
我们专注于被传统观念视为"无法治愈"或"极难治愈"的疾病与痛苦。这里没有标准答案,唯有对痛苦最深的回应。
我们汇聚前沿AI与跨学科智慧,深入每一个复杂病例的核心,重新梳理每一种治疗可能,为看似无解的难题,开创全新的解决路径。
"我们的存在,即是为了成为患者最后一站之后,
那束不可或缺的光,与坚实的新起点。"
破解数据孤岛与生物复杂性双重挑战,重塑从靶点发现到临床验证的研发范式
原生集成14+国际主流生物信息学平台,无缝打通基因组、蛋白组、影像组等多尺度数据,构建可追溯、可计算的生物数据资产库
千亿参数生命科学大模型融合因果推理与联邦学习,模拟体内生物过程,提供可解释的预见性决策,超越传统相关性分析局限
支撑干湿实验闭环迭代,缩短从早期发现(Hit)到临床候选物(PCC)的转化路径,提供监管科学友好的完整证据链

整合多组学数据分析与AI驱动的药物发现,为生物医药研发提供全方位支持
整合基因组学、转录组学、蛋白质组学、代谢组学和空间组学数据,提供全面的数据分析视角
整合14+主流生物信息学工具,提供统一的API接口和用户界面,简化分析流程
基于机器学习和深度学习的AI引擎,支持多组学数据分析和药物发现
提供丰富的数据可视化和交互式探索功能,帮助理解复杂的生物数据
支持团队协作和知识共享,提高研发效率和成果复用
基于微服务架构,支持功能扩展和定制化开发
我们的世界模型技术将AI与生物医药领域知识深度融合,构建了一个动态学习的智能系统,打造了全新的多模态生命科学世界模型。
整合全球权威数据库与文献资源
每日自动同步最新研究成果
显著提升预测准确性与可靠性
大幅缩短研发周期与降低成本

构建覆盖全面的生物医学知识图谱,整合基因、蛋白质、化合物、疾病等多维度实体及其复杂关系网络,为AI提供系统性的领域知识支撑
世界模型能够从海量研究论文、临床试验数据和实时监测数据中持续学习,自动更新和完善知识体系,确保知识的前沿性与准确性
融合基因组学、转录组学、蛋白质组学、代谢组学、影像组学等多种数据模态,构建全方位的生物医学世界模型,提供更准确的预测和分析
基于世界模型进行虚拟实验和预测,显著提升预测准确性,大幅加速药物发现过程,有效降低研发成本并提高成功率
通用分子设计世界模型,实现蛋白质、核酸、小分子等多形态分子的统一设计,显著提升设计效率,大幅缩短计算设计周期
基于自然语言理解的生物医学知识智能检索,快速获取相关研究成果和数据
辅助研究人员发现新的科学假设和研究方向,加速科学发现过程
基于多模态数据的预测分析,预测药物疗效、疾病风险和治疗反应
优化实验设计方案,提高实验效率和成功率,降低研发成本
基于世界模型技术,实现蛋白质、核酸、小分子等多形态分子的统一设计
通过交互式3D可视化探索复杂的生物数据关系
通过3D可视化技术,直观展示基因组、转录组、蛋白质组和代谢组之间的复杂关系,帮助研究人员发现新的生物标志物和药物靶点。
原生集成国际主流生物信息学平台,无缝打通多组学数据壁垒
用于空间转录组数据分析的综合工具包,支持从原始数据处理到高级可视化的完整工作流程
用于存储和处理空间生物学数据的统一框架,支持多种空间数据类型和格式
用于整合和分析多组学数据的平台,支持基因组学、转录组学、蛋白质组学和代谢组学数据的联合分析
生物信息学云平台,提供丰富的分析工具和流程,支持从数据上传到结果下载的一站式分析
基于Shiny的交互式多组学数据分析和可视化工具,支持多种图表类型和数据探索功能
用于多组学数据整合和分析的R包,支持变量选择、分类和预测等多种分析功能
多组学因子分析工具,用于从多个组学数据集中提取共享和特定的变异来源
用于分析基因组学和代谢组学数据之间关联的工具,支持识别潜在的生物标志物和药物靶点
代谢组学数据分析平台,支持代谢物识别、定量分析、 pathway分析和生物标志物发现
用于代谢物来源分析的工具,支持识别和定量分析生物样本中的代谢物来源
基因组学分析工具,支持DNA测序数据处理、基因表达分析、变异检测和注释等功能
用于分析基因组学数据的云平台,支持基因表达分析、变异检测和关联分析等功能
化合物与转录组桥梁,高效多组学数据分析工具,集成7种相关系数计算和因果关系建模方法,特别擅长基因-代谢物关联挖掘
通用分子设计世界模型,实现蛋白质、核酸、小分子等多形态分子的统一设计,设计效率较同类模型提升近50倍
基于机器学习和深度学习的AI引擎,提升生物医药产业效率

我们的AI引擎整合了先进的机器学习和深度学习算法,能够分析海量的生物数据,预测药物靶点,设计新的分子结构,并优化临床试验方案,全面提升生物医药产业效率。
利用深度学习算法分析多组学数据,预测潜在的药物靶点,提高靶点发现的效率和准确性
使用机器学习模型对大规模化合物库进行虚拟筛选,识别具有潜在活性的候选化合物
通用分子设计世界模型,实现蛋白质、核酸、小分子等多形态分子的统一设计,显著提升设计效率
AI辅助的临床试验方案设计和优化,提高临床试验的成功率和效率
通过AI辅助的靶点发现、虚拟筛选和分子设计,显著缩短药物研发周期。传统方法需要数年的研发流程,借助AI技术可在更短时间内完成,大幅提升研发效率。
AI模型通过多维度数据分析和预测,显著提升药物研发成功率。通过精准预测和智能决策,有效降低研发风险和成本,提高项目成功率。
利用深度学习算法分析多组学数据,精准预测潜在药物靶点,显著提高靶点发现的准确性和效率
使用机器学习模型对大规模化合物库进行快速虚拟筛选,大幅提升筛选效率,快速识别具有潜在活性的候选化合物
AI辅助的临床试验方案设计和患者招募优化,提高临床试验的成功率和执行效率
精心设计的用户界面,简化复杂的生物信息学分析流程,提高研究效率
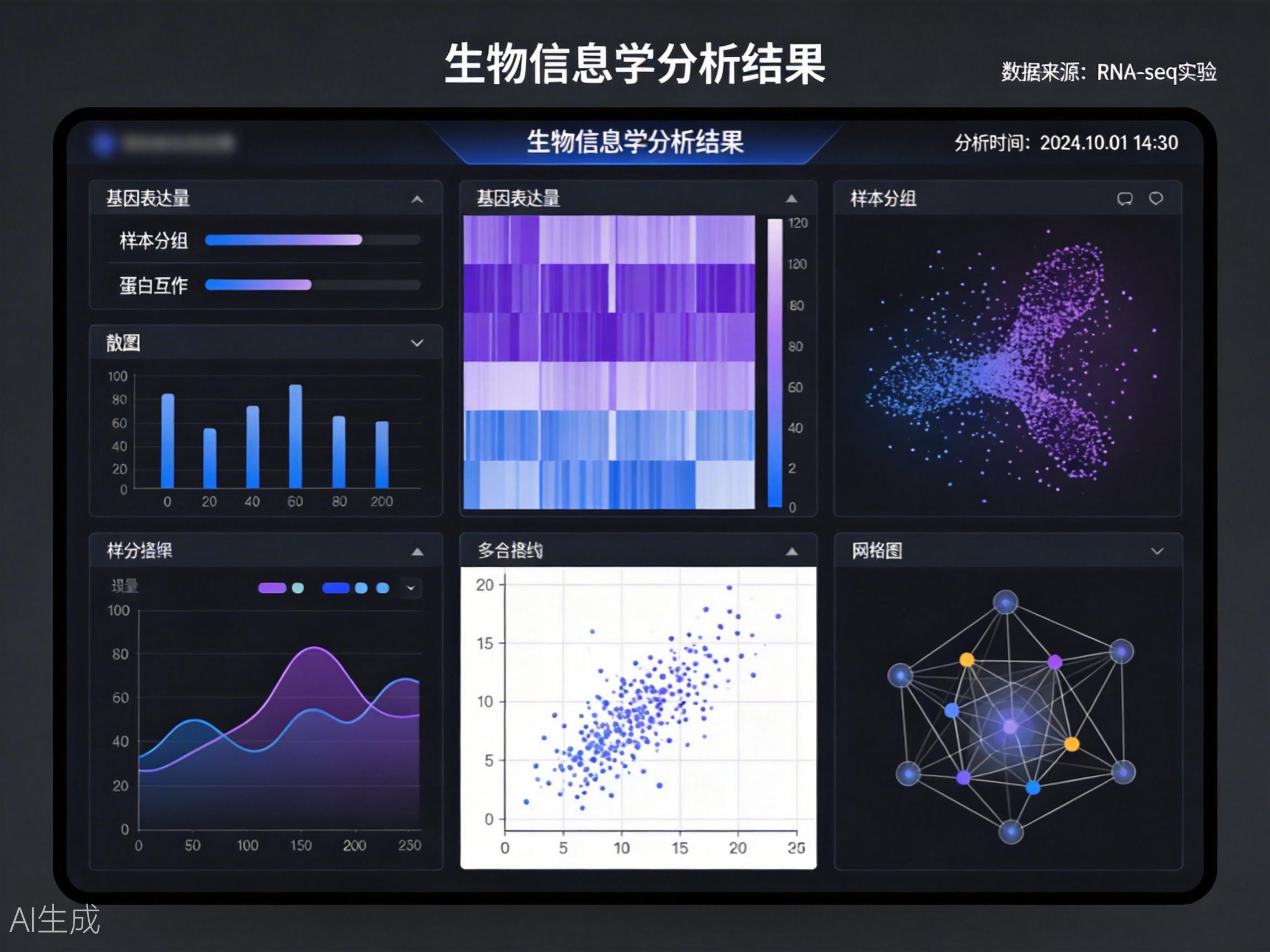

我们的用户界面设计遵循"以用户为中心"的理念,通过直观的布局和交互,让复杂的生物信息学分析变得简单易用。无论您是经验丰富的生物信息学家还是初入行的研究人员,都能快速上手并高效完成分析任务。
采用模块化设计,将复杂的分析流程分解为简单的步骤,引导用户完成整个分析过程
丰富的交互式可视化工具,帮助用户理解复杂的数据关系和分析结果
支持用户根据自己的需求定制分析工作流,提高分析效率和灵活性
完全响应式设计,支持在各种设备上使用,随时随地进行数据分析
直观展示项目进度、数据概览和最近分析结果,帮助用户快速了解项目状态
集中管理所有数据文件,支持数据上传、下载、预览和组织,方便数据管理和共享
集成12+生物信息学工具,提供统一的用户界面,简化分析流程
提供丰富的数据可视化工具,支持交互式数据探索和结果展示
提供AI模型训练、预测和优化功能,支持自定义模型和参数
支持团队协作和知识共享,提供讨论、评论和反馈功能
AI驱动的生物医药研发工作流程,从基础研究到临床应用,全程加速
利用AI分析多组学数据,识别潜在的药物靶点
对大规模化合物库进行虚拟筛选,识别潜在活性化合物
基于AI的分子设计和优化,创造新的药物分子
AI辅助的临床前研究设计和优化
AI优化的临床试验设计和患者招募
利用AI分析多组学数据,识别潜在的药物靶点,并通过实验验证其有效性和安全性。
对大规模化合物库进行虚拟筛选,识别潜在活性化合物,并利用AI设计新的分子结构。
进行体外和体内实验,评估药物的有效性、安全性和药代动力学特性。
设计和执行临床试验,评估药物在人体中的安全性和有效性。
药物上市后,持续监测其安全性和有效性,收集真实世界数据。